생명 위급하거나 대체 치료수단 없을 때 '사용 허용'
단 방사성의약품(루테슘) '안전성' 검증되지 않아 제외
미국 등서 허가받은 루타테라와 '제조원, 원료약과 분량 등 다르다'
[보건타임즈] '임상시험 약의 치료목적 사용승인' 건수가 올해 7월말까지 398건으로 지난해 같은 기간대비 비슷한 것으로 나타났다.(자료)
임상용 의약품은 품목허가 전 '비임상'을 거쳐 최소한의 안전성이 검증돼 국내 ‘임상시험’을 승인해준 약이다.
비임상시험은 사람에게 시험하기 전에 동물 등을 사용해 독성 등의 안전성을 검증하기 위해 실시하는 시험이다.
의약품 임상시험은 안전성-유효성을 입증하기 위해 사람을 상대로 임상적 효과 등을 확인하는 시험이다.
현재 식약처는 생명이 위급하거나 대체 치료수단이 없는 환자들의 치료기회를 확대하기 위해 임상시험용의약품을 품목허가 받기 전에 예외적으로 사용할 수 있도록 허용하는 ‘치료목적 사용승인’ 제도를 운영하고 있다.
식약처에 따르면 올해 '임상시험 약의 치료목적 사용승인' 건수는 7월말 현재 398건으로 지난 2016년 793건, 지난해 703건과 비교해 비슷한 수준이다.
이 제도가 첫 시행된 2002년부터 올해 7월까지 승인된 건수는 모두 4,842건이다.
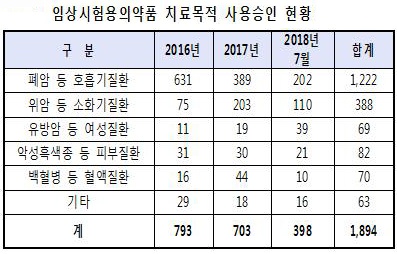
임상 약 사용건수는 폐암 등 호흡기질환(202건)에 가장 많았다.
다음으로는 위암 등 소화기질환(110건), 유방암 등 여성질환(39건), 악성흑색종 등 피부질환(21건), 백혈병 등 혈액질환(10건), 기타 질환(16건) 등의 순이었다.
단 국내에서 개발하는 방사성의약품(루테슘, Lu177)은 보건복지부 예산을 지원받아 동물실험 등 연구 진행 중에 있으며, 임상시험 승인을 받지 않아 최소한 요구하는 안전성이 검증되지 않은 물질로서 '치료목적 사용승인' 대상에서 아예 제외돼 있다.
루테슘(Lu177)에 도타테이트를 결합시켜 개발 중인 방사성의약품 '신경내분비종양치료제'는 미국 등에서 허가받은 의약품(루타테라Ⓡ)과는 제조원, 원료약품과 분량 등이 다르다.
식약처처럼 미국(Expanded Access Program)과 유럽(Compassionate use) 등도 자국 내에서 '임상시험' 승인을 받은 의약품에 한해 생명이 위급하거나 대체 치료수단이 없는 환자들의 치료기회를 주기 위해 사용토록 허용하고 있다.
식약처는 지난해 8월부터 환자나 보호자가 승인받은 임상시험용의약품의 코드명, 대상 질환, 사용되는 병원 등을 손쉽게 확인할 수 있도록 '치료목적 사용승인' 현황을 홈피를 통해 공개해오고 있다.