[보건타임즈] 식품의약품안전처(처장 이의경)는 코로나19 진단시약 긴급사용승인 신청과 관련, 질병관리본부를 통해 1월 28일부터 2월 28일까지 42개 업체에서 총 64건을 신청했다고 밝혔습니다.
이중 19건은 검토가 완료되어 4건은 긴급사용 승인, 6건은 성능미흡으로 부적합, 1건은 임상성능평가 불가, 8건은 업체가 신청을 취하 했다.
현재 45건은 검토가 진행 중이며, 8건은 질병관리본부에서 임상성능평가 예정, 8건은 식약처 검토결과 평가자료 보완 중, 29건은 식약처에서 서류 검토 중이다.
‘긴급사용 승인제도’는 감염병 대유행이 우려되어 의료기기(진단시약 등)의 긴급한 사용이 필요하나 국내에 허가제품이 없거나 공급이 부족한 경우, 중앙행정기관(질병관리본부 포함)이 요청한 제품의 허가를 면제해 한시적으로 제조(수입)․판매․사용할 수 있게 하는 제도다.
식약처는 질병관리본부와 협력해 ①서류검토(식약처) ②임상성능평가(질본) 및 ③전문가 검토(대한진단검사의학회) ④승인요청(질본) 및 승인(식약처) 4단계 검토절차를 거쳐 승인하고 있다.
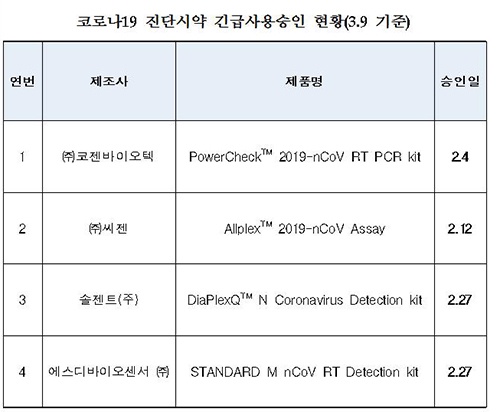
현재, 긴급사용 승인된 코로나19 진단시약 4개 제품은 모두 국내 의료기기 제조업체에서 생산되며, 3월 9일 기준 15,971 kit(522,770명 분량)이 생산되어 이중 11,478 kit(381,500명 분량)이 공급됐고 4,493kit (141,270명 분량)은 해당 업체에서 재고로 보유중이다.
정부는 현재 서류검토중인 제품에 대해서는 순차적으로 검토를 완료할 예정이며, 임상성능평가 및 전문가 검토 등 모든 절차가 완료되어 적합한 제품에 대해서는 검토가 완료되는 즉시 지속적으로 승인할 예정이다.