3일 '10월 허가심사 결과(허가보고서)' 발표

[보건타임즈] 지난 10월 의약품 13개, 의약외품 5개 총 18개 품목(신규허가 16개, 변경허가 2개/품목명단)이 식약처의 허가를 받았다.
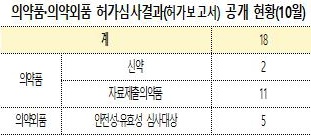
식약처는 의약품과 의약외품 허가심사의 투명성, 일관성, 신뢰성을 강화하기 위해 ▲ 신약 ▲ 자료제출의약품 ▲ 안전성·유효성 심사대상 의약외품을 공개하도록 한 약사법 제88조의2, 의약품 등 안전규칙(총리령) 제102조의8에 의거 지난 10월에 허가심사 결과(허가보고서)를 순차적으로 공개한다며 이같이 발표했다.
이중 대표 의약품으로는 동등생물의약품(바이오시밀러) '유플라이마펜주40㎎/0.4mL(아달리무맙, 유전자재조합)(㈜셀트리온)와 신약인 '지셀레카정100㎎(필고티닙말레산염)(한국에자이㈜)이 있다.
유전자 재조합의약품 '아달리무맙' 제제는 국내에서 첫 번째로 개발된 삼성바이오에피스㈜의 '아달로체프리필드시린지주40㎎(아달리무맙)'에 이어 두 번째로 개발된 동등생물의약품이다.
식약처는 앞으로 의약품과 의약외품의 허가심사 결과를 공개, 매월 공개 목록을 제공함으로써 제약업계의 제품 연구·개발에 도움이 될 수 있도록 노력하겠다고 밝혔다.