금연치료보조제 '바레니클린 의약품 단계적 안전관리'
불순물 저감화 이전까지 한시적 'NNV 185ng/일 이내' 제품만 '국내 출하·유통'
임의 복용 중단 없이 의․약사 상담 이후 '지속 복용 여부 등' 결정 권고
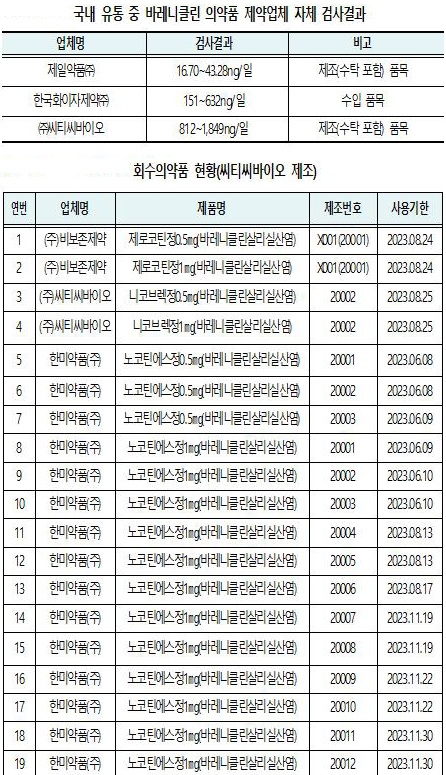
[보건타임즈] 이미 시중에 유통 중인 금연치료보조제 바레니클린 의약품 가운데 NNV 검출량이 733ng/일을 초과한 모든 제품은 제조업체가 자발적으로 회수한다.
이 조치는 ▲ 바레니클린 의약품 중 NNV 인체 영향평가 결과 위해 우려가 거의 없는 점 ▲ 금연치료보조제의 공급 차질이 우려되는 점 ▲ NNV 검출이 전 세계적인 상황 속에서 미국 등 주요 국가가 유통 중인 제품에서 733ng/일 이내로 검출된 제품(제조번호)은 회수 등 조치 없이 유통을 허용한다는 점 ▲ 중앙약심 자문 결과 등을 종합적으로 검토해 결정한 것이다.
이에 따라 ㈜씨티씨바이오가 제조(수탁 포함)한 3개 업체 6개 품목(표)의 모든 제조번호는 자발적 회수된다.
또 금연치료보조제 바레니클린 의약품은 한시적으로 185ng/일 이하인 제품만 국내 시중에 출하할 수 있게 된다.
이에 적용되는 '바레니클린' 성분의 '한시적 출하허용기준'을 185ng/일로 미국이 한시적으로 설정한 출하허용기준과 같은 수준이다.
식약처는 금연치료보조제 '바레니클린' 성분 함유 의약품 중 니트로사민 계열 불순물[N-nitroso-varenicline(엔-니트로소-바레니클린), 이하 NNV]의 안전성 조사 결과 인체 위해 우려는 매우 낮은 수준이라며 이같이 밝혔다.
다만 NNV가 국내 유통 중인 모든 제품에서 검출됨에 따라 ▲ 복용 환자에 대한 영향평가 ▲ NNV 1일 섭취허용량 설정·검출량별 조치 기준 ▲ 전문가와 환자 안내 사항 등 단계적인 안전관리 대책을 마련, 시행 중이다.
국내 바레니클린 의약품에서 NNV가 매우 낮은 수준으로 검출(16.70~1,849ng/일)됐으며, 인체 영향평가 결과 건강이 미치는 영향이 우려되지 않을 정도의 매우 낮은 것으로 나타났다면서 NNV 검출량은 추가로 암이 발생할 가능성이 10만 명 중 0.194~0.391명으로 확인됐다는 게 식약처의 설명이다.
식약처에 따르면 바레니클린 의약품을 복용한 환자의 인체 영향평가는 ▲ 국내 유통 중 제품의 일일 최대복용량 ▲ NNV 검사결과 ▲ 국민건강보험공단의 금연치료지원사업에 참여한 환자의 실제 투약 일수 등을 종합적으로 고려해 의약품 분야 국제 가이드라인 ICH M7(International Council for Harmonisation Mutagenic 7)에 따라 수행했다.
의약품 분야 국제 가이드라인에 따르면 10만 명 중 1명 이하인 경우는 ‘무시할 수 있는 수준’에 속한다는 것이다.
식약처는 중앙약심(중앙약사심의위원회)의 자문받아 화학구조가 매우 유사한 니트로사민 계열 물질 NTHP(N-Nitroso-1,2,3,6-tetrahydropyridine)의 독성 값 등을 참고해 NNV의 1일 섭취허용량을 37ng/일(미국 등 해외 규제기관과 같은 수준)로 설정했다.
NNV의 1일 섭취허용량이란 사람이 매일 평생(70년) 섭취할 때 자연 발생적인 발암 가능성 이외에 10만분의 1 확률로 암이 추가 더 발생할 수 있는 1일 섭취허용량을 의미한다.
식약처의 이러한 결정은 ▲ 바레니클린 의약품 중 NNV 인체 영향평가 결과 위해 우려가 거의 없는 점 ▲ NNV 검출량을 이번에 설정한 1일 섭취 허용량(37ng/일) 이하로 단번에 저감화하려면 제조공정 변경·평가에 시일이 걸리는 어려운 점 ▲ 미국에서 한시적 출하허용기준을 185ng/일로 설정한 점 ▲ 금연치료보조제의 환자 접근성 ▲ 중앙약심 자문 결과 등을 종합적으로 검토해 내렸다.
식약처는 NNV 검출량을 1일 섭취허용량 이하로 최대한 신속하게 저감화할 수 있도록 제조업계와 지속해서 의사소통, 협력체계를 유지하며 저감화가 완료되면 조사한 결과를 추가 발표할 계획이다.
이와 함께 식약처는 바레니클린 성분의 금연 치료 보조제(제조번호)를 처방받은 환자들은 의약품 복용을 임의로 중단하지 말 것과 계속 복용하거나 대체 의약품으로 전환 필요성 등은 반드시 의․약사와 상담하기를 권고했다.
상담 결과 대체 의약품으로 전환이 필요할 땐 국민건강보험공단의 금연치료지원사업 참여의료기관(2021년 기준, 15,085곳)에서 금연치료보조제 처방을 받은 후 약국에서 조제 받을 수 있다.
이때 1년에 3번(차수), 차수별 8주∼12주 동안 6회 이내 진료·상담·의약품 등의 비용만 환자 본인 부담금의 최대 100%까지 지원받을 수 있다.