식약처, ‘지난해 승인현황 분석-43개 시험기관 1차 차등평가 결과’ 공개
지난해 전체 임상시험계획의 승인건수는 607건으로 전년도 670건과 비교해 약 9.4%정도 감소했다.(자료/ ☞ http://www.bktimes.net/data/board_notice/1392084959-65.pdf)
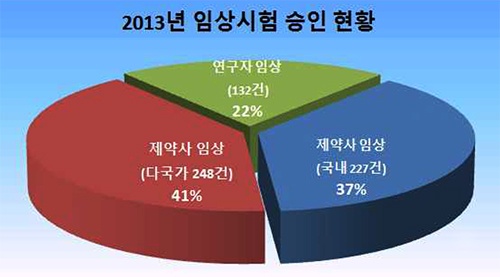
반면 최근 4년간 국내 제약사의 임상시험은 지속적인 증가 추세를 보였지만 다국적 사의 다국가 임상시험은 신물질을 개발 후 고비용과 장기간 소요, 낮은 성공률 등으로 지난해의 경우 248건이 승인돼 전년 290건 대비 14%가 줄었다.
식약처(처장 정승)는 지난해 임상시험계획 승인현황을 분석한 결과, 최근 몇 년간 계속된 전 세계적인 경기침체와 불황으로 다국적 제약사의 연구·개발(R&D) 비용이 줄어든 데다 국내 연구자들이 연구비를 확보하지 못하면서 다국가 임상과 연구자의 임상시험이 감소한데 따른 것으로 분석된다고 11일 밝혔다.
이중 가장 눈에 띤 부문은 연구자 임상시험이다
연구자 임상시험의 경우 지난해 132건으로 전년도 172건에서 20% 이상 급감했다.
그러나 국내 제약사의 임상시험은 전반적인 임상시험 감소에도 2012년 208건에서 2013년 227건으로 9.1% 늘어났다.
지난해 승인된 임상시험의 주요특징은 ▲국내 제약사의 임상시험 증가 추세 지속 ▲다국적 제약사와 연구자임상시험 감소 ▲효능 군별로는 종양, 심혈관계, 내분비계 등에 집중 ▲국내 제약사와 다국적 제약사 임상시험 분야 상이 ▲수도권․대형병원 편중현상 등이다.
<국내 제약사 임상시험 증가 추세>
임상 ‘2010년(140건) → 2011년(209건) →2012년(208건) → 2013년(227건)’
‘3상 승인건수 2010년 31건 →2011년 41건 →2012년 47건) →2013년 58건’
최근 4년간 국내 제약사의 임상시험은 2010년 140건 → 2011년 209건 →2012년 208건 → 2013년 227건으로 해마다 계속 증가세를 보여 왔다.
임상단계별로는 2010년 이후 1상에서 성과를 보인 개발 의약품들이 2~3상으로 진입하면서 최근 4년간 꾸준히 늘어났다.
이에 비례 3상 시험 승인건수도 2010년 31건 →2011년 41건 →2012년 47건) →2013년 58건으로 상승곡선을 그려왔다.
이러한 추세는 국내 제약사들이 지속가능한 성장을 위해 제네릭 개발 대신, 성인병 등 만성 질환을 대상으로 한 개량 신약 등의 개발이 필요하다는 판단에 따른 것으로 풀이된다.
<다국가임상 전년 대비 감소>
다국적사 국내 임상 248건 전년 290건 대비 무려 ‘14% 감소세’
임상비중 ‘3상 154건〉2상 65건〉1상 25건’ 順
이와 달리 지난해 다국가 임상은 전년 대비 크게 줄었다.
전 세계를 대상으로 다국적 제약사가 실시하는 다국가 임상시험은 신물질 연구에 들어가는 자금과 오랜 시간이 부담되거나 소요되는데다 성공할 확률이 낮아 R&D비용을 줄이면서 개발 가능성이 높은 의약품에 눈을 돌려 투자가 줄어 지난해 248건이 승인돼 전년 290건 대비 무려 14%나 감소세를 나타냈다.
하지만 다국가 임상시험은 3상(154건) 〉2상(65건) 〉1상(25건)순으로 여전히 초기 임상보다 3상비중이 높았다.
국내에 진출한 다국적 제약사들은 국내 임상시험 수행능력을 선진국 수준으로 평가하고 있으며, 들어가는 비용이 선진국의 80~90% 수준이어서 한국을 선호하고 있다는 게 식약처의 시각이다.
<국내 제약사와 다국적 제약사간 임상 분야 상이>
최근 국내 제약사와 다국적 제약사간 임상 분야가 다른 것도 눈에 띤다.
다국적 제약사의 경우 지난해 임상시험 승인된 의약품이 종양(101건), 심혈관계(20건), 내분비계(19건), 중추신경계(19건), 항생제(18건) 등에 집중한 반면 국내 제약사는 심혈관계(56건), 내분비계(30건), 중추신경계(19건), 소화기계(18건), 비뇨기계(15건)에 치중, 차이를 드러냈다.
지난해 임상시험 승인된 의약품을 효능 군별을 들여다보면 다국적 사가 개발에 초점을 둔 종양이 157건으로 가장 많았다.
다음으로는 국내제약사가 투자가 두드러진 심혈관계(80건), 내분비계(51건), 중추신경계(46건) 등의 순으로 천문학적 비용과 시간이 소요되는 신물질 개발보다는 비용 대비 높은 성공률의 개량 신약 개발에 집중하는 경향을 보이고 있다.
제제별로는 합성의약품이 72%, 바이오의약품 25%, 생약(한약)제제 3% 순이었다.
<제약사별 임상시험 승인 현황>
임상승인 최다 제약사는 ‘한국노바티스 28건, GSK 20건’
국내 제약사는 ‘일동제약 15건, 종근당 14건, 한미약품 12건 순’
지난해 임상시험 승인을 가장 많이 받은 다국적 제약사는 한국노바티스 28건, 글락소스미스클라인 20건 등의 순으로 나타났다.
임상시험자로부터 위임받은 연구개발 수탁전문기업(CRO Contract Research Organization)으로는 퀸타일즈 트랜스내셔널코리아(25건), 피피디 디벨럽먼트피티이엘티디(17건) 등이었다.
국내 제약사의 경우 일동제약이 15건으로 가장 많았으며 종근당 14건 한미약품 12건 등이 뒤를 이었다.
연구자 임상은 서울대병원 24건, 삼성서울병원 19건 등으로 많았다.
<지역·기관 편중현상 여전>
서울-경기도 전체 임상의 ‘약 70%’ 차지
빅 5병원 점유율은 ‘35.8%’
이와 함께 지역·기관의 편중현상은 여전했다.
서울 55%, 경기도 17%가 약 70%를 차지했으며 나머지는 부산 6%, 대구 5%, 인천 4%, 전라도 3% 등의 순이었다.
임상시험 실시기관도 서울대병원(197건, 8.1%), 삼성서울병원(196건, 8.1%), 서울아산병원(186건, 7.7%), 연세대 신촌세브란스병원(161건, 6.6%), 가톨릭대 서울성모병원(130건, 5.3%) 등으로 이들 5개 대형 병원의 점유율이 35.8%를 차지했다.
식약처는 지난해 도입된 차등관리제에 따라 지난해 임상시험 수행건수가 많은 병원 등 43개 임상시험 실시기관을 대상으로 수행능력을 평가한 결과, ‘가톨릭대 서울성모병원’ 등 28개 기관이 ‘우수(A등급)’, ‘강동경희대학교의대병원’ 등 15개 기관이 ‘보통(B등급)’으로 평가됐다고 밝혔다.
차등관리제는 임상시험 실시기관의 수행능력을 평가, 3등급으로 나눠 점검항목‧주기를 차별화(우수(A등급) 1회/5년, 보통(B등급) 1회/3년, 미흡(C등급) 2회/년)하는 사후관리 제도다.
식약처는 나머지 120여개 임상시험 실시기관에 대해선 내년까지 연도별 60개 기관의 평가를 마친 뒤 2016년부터 평가등급에 따라 점검주기 등을 차별화하는 등 체계적이면서 효율적인 사후관리를 실시, 임상시험기관의 관리 수준을 향상시켜 나갈 계획이다.