2일 '의약품 등 안전규칙개정안' 입법예고
생동 '임상시험과 실시기준, 준수사항 등 통합' 운영
의약외품 첨부 문서에 '효능과 효과 등 표기' 의무화

[보건타임즈] 앞으로 외국 제약사가 국내 제약사에 제제기술을 이전한 재심사 대상 의약품과 희귀의약품 등으로 국내 제조시설 없이도 위탁제조판매업 신고를 해야 된다.
재심사는 의약품 허가 후 일정기간(허가일로부터 4∼6년)을 정해 시판 후 약효의 안전성·유효성을 평가하는 제도다.
대상은 신약, 투여경로 변경(예 주사제→정제) 전문의약품, 유효성분 종류, 배합비율이 다른 전문의약품(예 단일제→복합제)등이다.
위탁제조판매업은 국내에 제조시설을 갖추지 않았더라도 식약처장으로부터 제조판매품목허가를 받은 의약품을 국내 제조업자에게 위탁, 제조 판매하는 영업을 말한다.
이를 통해 이들 품목의 시판허가를 받을 수 있다.(아래 표 참조)
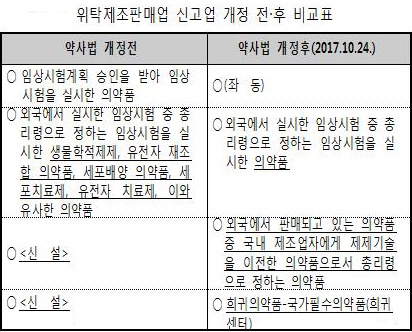
식약처는 이 같은 내용을 골자로 한 의약품 등 안전 규칙개정(안)을 입법예고한다고 밝혔다.
이 조치는 지난해 10월 개정‧공포된 약사법에 의거 하위법령을 개정, 정비하기 위한 것이다.
개정안은 해외 의약품의 우수한 제제기술을 국내에 이전, 국내 제약 산업의 경쟁력을 높이기 위해 마련됐다.
식약처에 따르면 이 개정안의 주요 내용은 ▲ 외국에서 판매되는 의약품 중 위탁제조판매업 신고 대상 ▲ '임상시험'과 '생물학적동등성시험'의 실시기준, 준수사항 등 통합관리 ▲ 의약외품 표시‧기재사항 강화 등이다.
이에 따라 외국 제약사가 해외에서 판매되는 의약품 중 국내 제약사에 제제기술을 이전한 재심사 대상 의약품 등의 위탁제조판매업 신고가 늘 것으로 보인다.
식약처는 이 제도를 통해 외국 제약사의 신약을 국내제약사에 위탁 제조할 수 있도록 해 국내 제약사는 공장 가동율을 높일 수 있을 것으로 내다봤다.
식약처는 '생물학적동등성시험'도 개선된다.
그간 ‘임상시험’과 별개로 실시기준, 준수사항 등을 정해 적용해왔으나, 앞으로는 임상시험과 통합, 효율적으로 운영한다.
이와 함께 소비자의 알권리를 강화하기 위해 의약외품의 첨부 문서에 효능·효과, 용법‧용량, 주의사항, 손상 제품의 연락처 또는 교환방법 등을 기재하는 것이 의무화된다.
식약처는 이를 통해 국내 제약 산업의 안정적 성장 기반이 확대되는 계기가 될 것이라며, 앞으로 국내 제약산업 강화를 위한 제도적 지원과 함께 우수한 의약품이 공급‧유통되는 환경을 조성하기 위해 최선을 다하겠다고 전했다.
자세한 내용은 통합입법예고시스템 또는 식약처 홈피→ 법령‧자료→ 입법/행정예고에서 확인할 수 있다.